Вы являетесь медицинским работником? Для полного доступа к медицинской информации войдите или зарегистрируйтесь.
 Опухоли с транслокациями NTRK
Опухоли с транслокациями NTRK
NTRK является значимым биомаркером и онкогенным драйвером при многих типах опухолей
Персонализированная медицина при лечении редких опухолей
Знание молекулярного профиля опухоли может открыть новые возможности таргетной терапии для лечения пациента. 1–3
С помощью высококачественного тестирования NGS можно понять, какие именно мутации определяют рост и уникальный молекулярный профиль опухоли.4
Что меняет персонализированная медицина?5,6
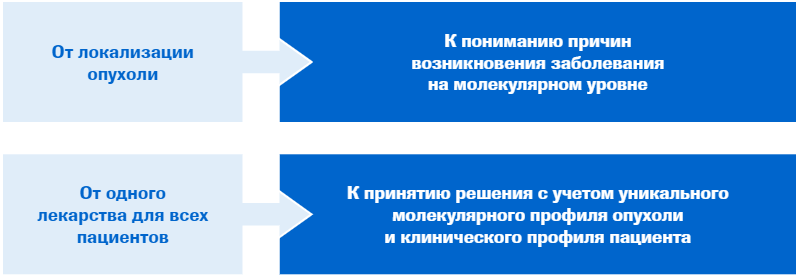
Для усовершенствования возможностей лечения пациентов со значимыми биомаркерами изучаются таргетные методы лечения7,8.
- Биомаркеры, такие как ALK, BRAF, EGFR, HER2, KIT и ROS1, изменили подход к терапии при лечении многих типов рака9–11
- Транслокации генов NTRK являются значимыми биомаркерами и онкогенами при более чем 25 типах опухолей7,8,12
Ген киназы анапластической лимфомы (ALK), транслокации которого обнаруживаются приблизительно в 5% опухолей при НМРЛ.13
Протоонкоген B-Raf (BRAF) обнаруживается в 1,5-3,5% опухолей при НМРЛ14 и в 8-12% случаев метастатического колоректального рака.15 Частота варьирует среди опухолей человека: от более чем 80% при меланоме до всего нескольких процентов (0-18%) в других типах опухолей.15
Ген EGFR — ген рецептора эпидермального фактора роста. При НМРЛ любой гистологии частоты мутаций EGFR варьировались в диапазоне от 8,4 до 35,9% у постоянных/заядлых курильщиков и от 37,6 до 62,5% у никогда не куривших/изредка куривших пациентов.16
Ген рецептора эпидермального фактора роста 2 типа (HER2), обнаруженный в 2% случаев аденокарциномы лёгкого17, гиперэкспрессия онкогена HER2 выявляется в 15-20% случаев первичного рака молочной железы.18
У пациентов с положительной экспрессией CD117/KIT (рецепторная тирозинкиназа, продукт гена KIT) в ткани опухоли при НМРЛ наблюдалась значительно более короткая безрецидивная выживаемость по сравнению с пациентами без экспрессии CD117/KIT.13,19
Транслокации с участием c-ros онокогена 1 (ROS1) являются терапевтической мишенью при НМРЛ и встречаются у 1-2% пациентов.20,21 Они также являюся полезными биомаркером при нескольких типах опухолей.22,23
Ген NTRK (нейротрофной тропомизин-рецепторная киназа) является значимым биомаркером и онкогенным драйвером.7,6,12 Транслокации NTRK встречаются у 0,3% пациентов при раличных типах солидных опухолей,24 включая: папиллярный рак щитовидной железы, НМРЛ, аналог секреторной карциномы молочных желез из слюнных желез, рак молочной железы, рак поджелудочной железы, колоректальный рак и саркомы (включая гастроинтестинальные стромальные опухоли).7,8,12
Продолжаются исследования по выявлению новых биомаркеров и таргетных препаратов, в том числе в отношении генов NTRK
Использование NGS высокого качества может принести пациентам большую клиническую пользу благодаря новейшим таргетным препаратам1,9,25,26
- Комплексное геномное профилирование использует технологию секвенирования нового поколения для широкого анализа генома опухоли и выявления всех клинически значимых изменений, потенциально расширяющих возможности лечения пациентов4,26–30
- Транслокации с участием генов NTRK и ROS1 могут быть точно определены с помощью комплексного геномного профилирования4,26–30
Персонализированная медицина сочетает в себе различные варианты лечения, в том числе традиционные методы химиотерапии и новые таргетные препараты для достижения наилучшего возможного результата для пациента.5
Прошедшие мероприятия по персонализированной медицине
ЦНС — центральная нервная система; NGS — секвенирование нового поколения; НМРЛ -немелкоклеточный рак легкого.
Ссылки:
- Rozenblum AB, et al. J Thorac Oncol 2017;12:258–268.
- Schwaederle M, Kurzrock R. Oncoscience 2015;2:779–780.
- Mansinho A, et al. Expert Rev Anticancer Ther 2017;17:563–565.
- Frampton GM, et al. Nat Biotechnol 2013;31:1023–1031.
- Bode AM, Dong Z. npj Precision Onc 2018;2:1.
- Roche.com. What is Personalised Healthcare all about? Available from: https://www.roche.com/about/priorities/personalised_healthcare/what_is_phc.htm (Accessed April 2019).
- Vaishnavi A, Le AT, Doebele RC. Cancer Discov 2015;5:25–34.
- Amatu A, Sartore-Bianchi A, Siena S. ESMO Open 2016;1:e000023.
- National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines). Non-Small Cell Lung Cancer. V.3.2019, 2019. Available at: www.nccn.org/professionals/physician_gls/recently_updated.aspx (Accessed April 2019).
- National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines). Breast Cancer. V.1.2019, 2019. Available at: www.nccn.org/professionals/physician_gls/recently_ updated.aspx (Accessed April 2019).
- National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines). Acute Myeloid Leukemia. V.2.2019, 2019. Available at: www.nccn.org/professionals/physician_gls/recently_updated.aspx (Accessed April 2019).
- Lange AM, Lo HW. Cancers (Basel) 2018;10.
- Baumgart M, Pandya K. Exp Rev Precis Med Drug Dev 2016;1:25–36.
- Leonetti A, et al. Cancer Treat Rev 2018;66:82–94.
- European Society for Medical Oncology. BRAF in Colorectal Cancer: ESMO Biomarker Factsheet. Available at: https://oncologypro.esmo.org/Education- Library/Factsheets-on-Biomarkers/BRAF-in-Colorectal-Cancer (Accessed April 2019).
- Dearden S, et al. Ann Oncol 2013;24:2371–2376.
- Tsao S, et al. J Thorac Oncol 2016;11:613–638.
- European Society for Medical Oncology. HER2 in Breast Cancer: ESMO Biomarker Factsheet. Available at: https://oncologypro.esmo.org/Education-Library/Factsheets-on-Biomarkers/HER2-in-Breast-Cancer (Accessed April 2019).
- Sakabe T, et al. Oncol Lett 2017;13:3703–3708.
- Bergethon K, et al. J Clin Oncol 2012;30:863–870.
- Dugay F, et al. Oncotarget 2017;8:53336–53351.
- Davies K, Doebele RC. Clin Cancer Res 2013;19:4040–4045.
- Lin J, Shaw A. J Thorac Oncol 2017;12:1611–1625.
- Okamura R, et al. JCO Precis Oncol 2018;2018.
- Gagan J, Van Allen EM. Genome Med 2015;7:80.
- Suh JH, et al. Oncologist 2016;21:684–691.
- Drilon A, et al. Clin Cancer Res 2015;21:3631–3639.
- Rankin A, et al. Oncologist 2016;21:1306–1314.
- Ross JS, et al. Cancer 2016;122:2654–2662.
- Hirshfield KM, et al. Oncologist 2016;21:1315–1325

