Вы являетесь медицинским работником? Для полного доступа к медицинской информации войдите или зарегистрируйтесь.
Диагностика рака от Roche
Свершившиеся открытия и перспективы будущего
Диагностические инновации позволяют вовремя поставить верный диагноз и подобрать персонализированное лечение. Рассказываем, как технологии меняют подход к диагностике рака и что в этой сфере может измениться в ближайшем будущем.
Делать передовую диагностику максимально доступной
Решения Roche Tissue Diagnostics ежегодно помогают 4,3 миллионам пациентов пройти тестирование по таким ключевым биомаркерам, как HER2, ALK, PD-L1 (и другим), открывая доступ к 19 персонализированным методам терапии — больше, чем у любого другого производителя ИГХ-тестов¹.
В 1985 году патолог, доктор медицины Томас Гроган основал компанию по разработке и производству гистопатологических диагностических систем Ventana Medical Systems — будущий отдел тканевой диагностики Roche. Уже к концу 1980-х прототип автоматического иммуногистохимического (ИГХ) окрашивания позволял получать результаты быстрее и стабильнее.
Roche приобрела Ventana в 2008 году. На этой базе возникла концепция компаньонных диагностических тестов (CDx) — когда анализ в лаборатории напрямую указывает, подойдет ли пациенту таргетная терапия 1. Первый такой тест был одобрен FDA еще в 1998 году и определял сверхэкспрессию HER2-рецепторов у пациенток с раком молочной железы ². Это позволило идентифицировать подгруппу больных, которым подходило новое на тот момент таргетное лечение, и стало поворотным моментом к эре персонализированной медицины.
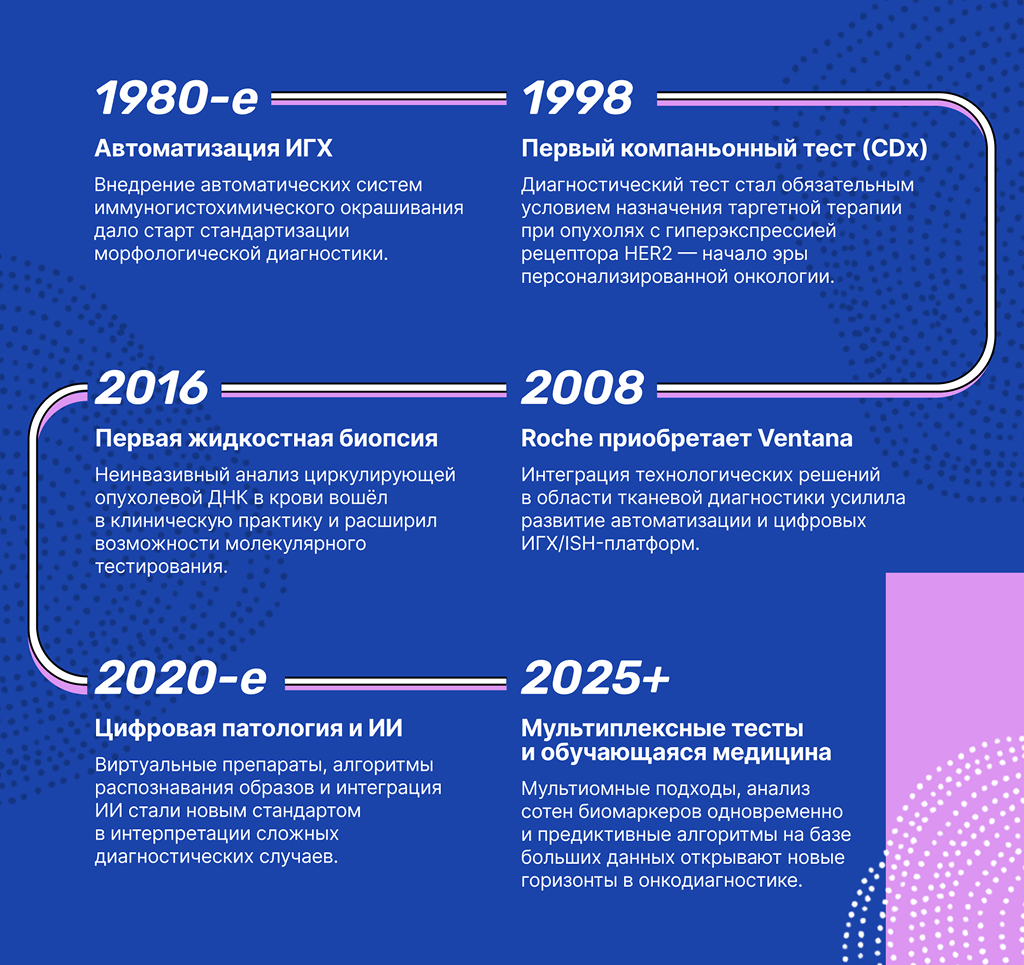
Компаньонные диагностикумы прочно вошли в онкологию: по данным FDA их уже более 60 только в онкогематологии ³ и Roche держит лидерство в этой сфере. Практически в каждом крупном онкоцентре сегодня стоят автоматические системы, которые выполняют иммуногистохимические и in situ гибридизационные анализы с высокой точностью и воспроизводимостью. Это означает, что независимо от того, где лечится пациент — в ведущей клинике или небольшом госпитале — уровень диагностической поддержки может быть одинаково высоким.
«…Медицина должна быть одинаково качественной во всем мире… Я не принимаю мнение, что барьером для этого служит экономика», — говорил Томас Гроган¹. Его слова стали частью философии Roche: делать передовую диагностику максимально доступной.
Персонализированная медицина: эволюция диагностических методов
Комплексное геномное профилирование опухоли — метод, возникший благодаря развитию секвенирования нового поколения (NGS). Он позволяет за один тест проанализировать сотни потенциально значимых мутаций в ДНК опухоли. Roche инвестировала в эту область, в том числе через сотрудничество со своей дочерней компанией Foundation Medicine. Результат — появление первых в мире диагностических панелей, охватывающих весь спектр онкогенетических изменений, официально одобренных регуляторами. Например, по обычной пробирке крови можно одновременно проанализировать более 300 генов, связанных с раком, и выявить мутации, которые заставляют опухоль расти4. Такой анализ позволяет быстрее поставить точный молекулярный диагноз и подобрать таргетную терапию под индивидуальный «мутационный портрет» опухоли.
Геномные тесты особенно востребованы при распространенных стадиях рака, когда стандартные методы терапии уже не работают. В таких случаях компаньонный ДНК-тест может определить, есть ли у пациента «лекарственная» мутация — например, в генах EGFR, BRAF, ALK, BRCA1/2 и многих других — и тем самым указать путь к современным таргетным препаратам либо к клиническим исследованиям новых лекарств.
За последние годы список таких тестов расширяется лавинообразно. Появляются новые категории. Пример — группа опухолей молочной железы с низкой экспрессией HER2, ранее считавшихся HER2-отрицательными. Для них нашлась своя таргетная терапия, и потребовались сверхчувствительные методы диагностики «HER2-low» статуса3. Компания разработала соответствующий ИГХ-тест и получила на него одобрение регулирующих органов2.
Жидкостная биопсия: анализ крови вместо скальпеля
Одно из достижений последних лет — развитие жидкостных биопсий, то есть методов выявления опухолевых маркеров по анализу крови: теперь не всегда нужна инвазивная процедура, чтобы узнать молекулярный профиль опухоли. Например, примерно у 20% больных немелкоклеточным раком легкого невозможно полностью выполнить нужные генетические тесты из-за нехватки или недоступности опухолевой ткани5. В таких случаях можно выполнить анализ плазмы крови на фрагменты опухолевой ДНК.
Еще в 2016 году Roche представила первый в мире FDA-одобренный жидкостный тест мутаций (для гена EGFR при раке легких) 6, 7, а сегодня доступны уже целые панели геномного профилирования по крови. Один из тестов исследует 324 гена по циркулирующей ДНК опухоли и выдает отчет с перечнем потенциально активных мутаций с оценкой доли ДНК опухоли в образце 4. Такой подход делает возможным полноценный молекулярный диагноз, когда опухоль сложно биопсировать повторно или времени на это нет. В ведущих мировых рекомендациях (ESMO, ASCO, NCCN) жидкостные тесты уже включены в стандарты ведения онкопациентов4.
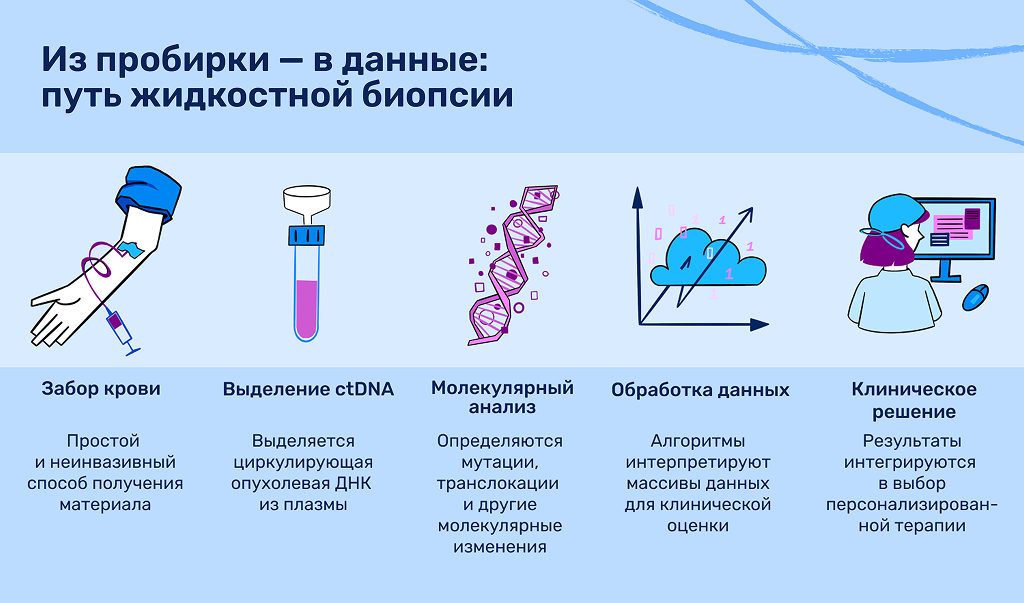
Жидкостная биопсия позволяет отслеживать эффективность лечения по динамике мутированной ДНК в крови и фиксировать появление резистентных к терапии клонов задолго до прогрессирования на КТ.
В перспективе раннее обнаружение рецидива с помощью анализа крови может кардинально изменить онкологию: вместо ожидания появления опухоли на снимках врачи смогут возобновлять лечение при первых же молекулярных признаках возвращения болезни.
Ведутся исследования, можно ли с помощью высокочувствительных методов искать следы рака у практически здоровых людей — проводить скрининг на основе анализа ДНК опухоли в крови.
Цифровая патоморфология и ИИ: новое «зрение» для диагностики
Цифровая патоморфология — это переход от просмотра стекол под микроскопом к сканированию препаратов и их анализу на компьютере. Roche была среди пионеров этого направления: подразделение Ventana разработало целую линейку сканеров высокого разрешения для гистологических стекол, и недавно они получили одобрение FDA для клинического использования в США3. Теперь врач может поставить диагноз, глядя на экран — причем консультировать могут специалисты из разных стран, параллельно рассматривая одно и то же цифровое изображение.
Диагностика рака: тогда и сейчас
| Направление | Раньше | Сейчас |
|---|---|---|
| ИГХ-окрашивание | Ручное | Автоматизированное и стандартизованное |
| Генетические тесты | Единичные мутации | Панели из сотен генов (NGS) |
| Биопсия | Инвазивная | Жидкостная биопсия из крови |
| Интерпретация | Врач вручную | Поддержка ИИ |
Оцифровка — лишь первый шаг. Следующий скачок связан с искусственным интеллектом (AI). Алгоритмы уже научились распознавать на цифровых препаратах мельчайшие признаки патологии. В 2024 году компания объявила о интеграции более 20 передовых AI-алгоритмов от разных разработчиков в открытую платформу цифровой патологии8. Эти алгоритмы охватывают самые разные задачи: от поиска микрометастазов в лимфоузлах до автоматического подсчета индекса Ki-67, от определения доли опухолевых клеток в образце до количественной оценки экспрессии рецепторов8.
Уже сейчас в некоторых лабораториях мира используются AI-модули для оценки иммуногистохимических тестов. Например, алгоритмы помогают стандартизовать подсчет PD-L1-позитивных клеток в опухоли легкого или мочевого пузыря — что критично для подбора иммунотерапии9. Другие программы специализируются на обнаружении митозов и делении опухоли по градации, третьи — на выявлении особых морфологических паттернов10. В будущем такие «цифровые коллеги» патологоанатома возьмут на себя рутинную работу по анализу изображений, позволяя врачу сконцентрироваться на самых сложных случаях.
В России цифровая патоморфология делает первые шаги. В 2010-х некоторые частные лаборатории и институты начали оцифровывать стекла для дистанционных консультаций и учебного процесса. К 2018 году были внедрены первые облачные платформы для удаленного анализа гистологических изображений11. В той же обзорной статье 2018 г. отмечалось, что в ряде российских лабораторий уже используются сканеры и наработки в области машинного обучения для распознавания изображений11.
Широкого перехода на полностью цифровой рабочий процесс пока нет — основной диагностический метод по-прежнему оптический микроскоп. Ограничения связаны с высокой стоимостью сканеров, необходимостью хранения больших объемов данных и отсутствием утвержденных нормативов. Однако интерес со стороны медицинских организаций растет: в 2024 году в московском университете развивается обучение виртуальной микроскопии студентов-медиков12. Регуляторных барьеров к использованию сканированных образцов в диагностике фактически нет, поэтому некоторые учреждения уже применяют их, особенно для консилиумов и вторых мнений. В рамках нацпроектов обсуждается создание централизованных хранилищ цифровых биобанков стекол13.
Ожидается внедрение систем поддержки принятия решений для патологоанатомов на основе ИИ11. Такие алгоритмы распознавания опухолевых клеток, подсчета митозов, оценки экспрессии ИГХ-маркеров сейчас проходят апробацию. В будущем, по мере накопления опыта, цифровая патология может существенно ускорить выдачу результатов и улучшить качество диагностики, особенно в отдаленных регионах, где не хватает узких специалистов.
Перспективы: диагностика завтрашнего дня
Ближайшее десятилетие может кардинально изменить облик онкологической диагностики. «Следующий этап — научиться предсказывать, ответит пациент на лечение или нет. А для тех, кто не ответит, — понять причину и подобрать альтернативу. Думаю, через 10 лет мы будем ставить диагнозы по препаратам с мультиплексным окрашиванием», — говорит Томас Гроган, основатель Ventana1.
«Мультиплексирование», о котором говорит Гроган, это одновременное выявление десятка и более различных маркеров на одном стекле. Такой срез будет светиться разными цветами, как картина импрессиониста 1, и разобраться в этой сложной мозаике поможет ИИ. Это откроет путь к принципиально новому уровню патоморфологии, когда за один шаг оцениваются десятки параметров опухоли — от состава иммунных клеток вокруг нее до активации разных сигнальных путей.
Еще одно важное направление — синтез диагностических данных и клинической информации. Компания развивает цифровые платформы, связывающие воедино результаты всех анализов пациента. Пример — система, помогающая врачебному консилиуму комплексно оценить данные по пациенту (гистология, молекулярный профиль, изображения КТ/МРТ, литература) и совместно выработать персонализированный план лечения. В перспективе подобные платформы смогут опираться и на большие данные: объединяя сведения от тысяч пациентов, алгоритмы будут подсказывать врачам, какие стратегии показали лучшие результаты для пациентов с похожим профилем. По сути, это реализация концепции обучающейся системы здравоохранения (learning healthcare system), где каждая новая история болезни улучшает подходы к следующим случаям.
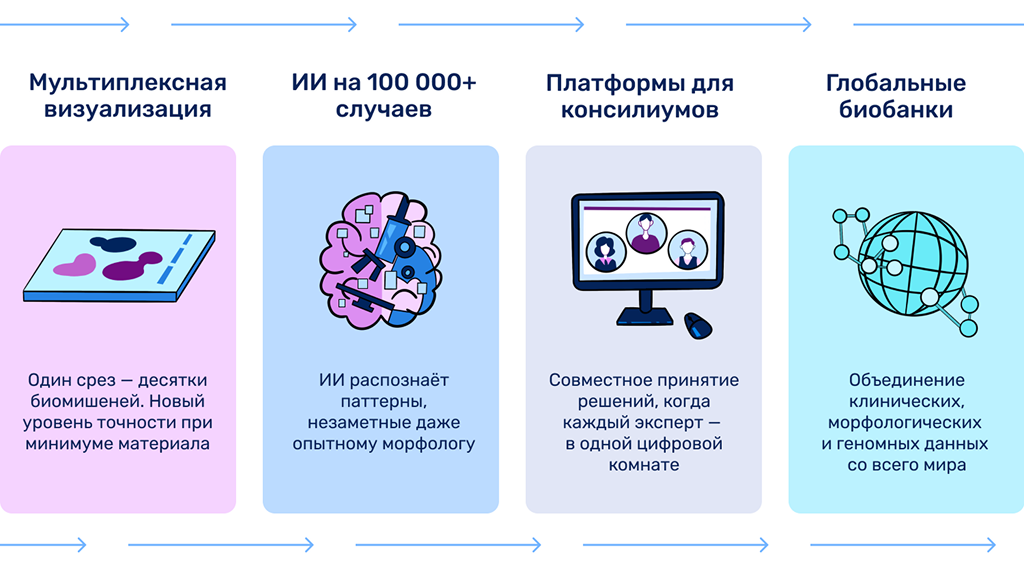
Диагностика становится неотъемлемой частью персонализированной борьбы с раком. Стратегия поиска чувствительных методов раннего выявления рака, новых молекулярных маркеров для трудноизлечимых опухолей, интеграции геномных, морфологических и клинических данных направлена на главную цель — сделать рак не смертельным приговором, а управляемым заболеванием.
Вам может быть интересно
Источники:
- Ventana Medical Systems and Roche Tissue Diagnostics change the pathology landscape over the last 40 years [Электронный ресурс] — Roche Diagnostics. — URL: https://diagnostics.roche.com/us/en/article-listing/ventana-medical-systems-and-roche-tissue-diagnostics-change-the-pathology-landscape-over-the-last-40-years.html (дата обращения: 27.07.2025).
- Oncology – Product Category [Электронный ресурс] — Roche Diagnostics. — URL: https://diagnostics.roche.com/us/en/products/product-category/health-topic/oncology.html — (дата обращения: 27.07.2025).
- 2025: the future of cancer diagnostics in the pathology lab [Электронный ресурс] — Roche Diagnostics. — URL: https://diagnostics.roche.com/us/en/article-listing/2025-the-future-of-cancer-diagnostics-in-the-pathology-lab.html — (дата обращения: 27.07.2025).
- Roche France, Foundation Medicine and the Institute Gustave Roussy announce unique partnership to provide in-house liquid biopsy genomic testing to cancer patients in France [Электронный ресурс] — Foundation Medicine. — URL: https://www.foundationmedicine.com/press-releases/roche-france%2C-foundation-medicine-and-the-institute-gustave-roussy-announce-unique-partnership-to-provide-in-house-liquid-biopsy-genomic-testing-to-cancer-patients-in-france — (дата обращения: 27.07.2025).
- Infographic: Journey of a Liquid Biopsy [Электронный ресурс] — Roche Diagnostics. — URL: https://diagnostics.roche.com/global/en/article-listing/infographic-journey-of-a-liquid-biopsy.html — (дата обращения: 27.07.2025).
- Kwapisz D. The first liquid biopsy test approved. Is it a new era of mutation testing for non-small cell lung cancer? Ann Transl Med. 2017 Feb;5(3):46. doi: 10.21037/atm.2017.01.32. PMID: 28251125; PMCID: PMC5326656.
- U.S. Food and Drug Administration. cobas EGFR Mutation Test v2 [Электронный ресурс] // FDA. — 2016. — URL: https://www.fda.gov/drugs/resources-information-approved-drugs/cobas-egfr-mutation-test-v2 (дата обращения: 22.01.2026).
- Roche advances AI-driven cancer diagnostics by expanding its digital pathology open environment [Электронный ресурс] — PR Newswire. — URL: https://www.prnewswire.com/news-releases/roche-advances-ai-driven-cancer-diagnostics-by-expanding-its-digital-pathology-open-environment-302241196.html — (дата обращения: 27.07.2025).
- van Eekelen L., Spronck J., Looijen-Salamon M. et al. Comparing deep learning and pathologist quantification of cell-level PD-L1 expression in non-small cell lung cancer whole-slide images // Scientific Reports. 2024. Vol. 14. Article number: 7136. DOI: 10.1038/s41598-024-57353-1
- P. Premananthan and M. Kanagarathnam, «Deep Learning-Based Mitosis Detection in Breast Cancer Histopathology Images: A Mapping Study,» 2024 International Research Conference on Smart Computing and Systems Engineering (SCSE), Colombo, Sri Lanka, 2024, pp. 1-5, doi: 10.1109/SCSE61872.2024.10550511.
- Цифровая патология в России: опыт и перспективы [Электронный ресурс] — Русский медицинский журнал. — URL: https://www.rmj.ru/articles/onkologiya/Cifrovaya_patologiya_vRossii_opyt_iperspektivy/ — (дата обращения: 27.07.2025).
- Цифровая эволюция: в Институте клинической морфологии и цифровой патологии внедряют в образовательный процесс ИИ [Электронный ресурс] — Сеченовский университет. — URL: https://www.sechenov.ru/pressroom/news/tsifrovaya-evolyutsiya-v-institute-klinicheskoy-morfologii-i-tsifrovoy-patologii-vnedryayut-v-obrazo/ — (дата обращения: 27.07.2025).
- Лебедев Г.С., Шадеркин И.А., Тертычный А.С., Шадеркина А.И. Цифровая патоморфология: создание системы автоматизированной микроскопии. Российский журнал телемедицины и электронного здравоохранения 2021;7(4);27-47; https://doi.org/10.29188/2712-9217-2021-7-4-27-47

