Вы являетесь медицинским работником? Для полного доступа к медицинской информации войдите или зарегистрируйтесь.
Мутации NTRK в детской онкологии
Сулейманова Амина Магомедовна
научный сотрудник, детский онколог НМИЦ онкологии им. Н.Н.Блохина
Семейство генов NTRK (нейротрофных рецепторных тирозинкиназ) включает три гена — NTRK1, NTRK2 и NTRK3. Данные гены кодируют тропомиозин-рецепторные киназы (TRK), регулирующие пролиферацию, дифференцировку и выживание нейронов в центральной и периферической нервной системе (Aepala 2022).
Существует три белка TrkA/B/C, которые кодируются тремя генами NTRK1/2/3 соответственно. При взаимодействии с факторами роста происходит димеризация и активация рецепторов. (Aepala 2022)
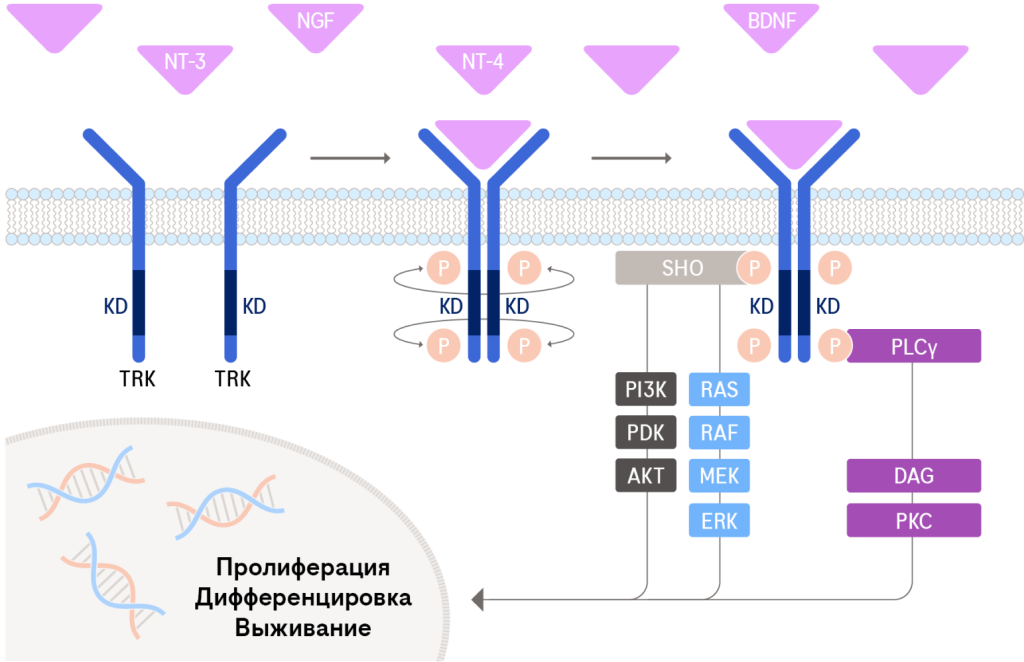
Почему генетические события приводят к малигнизации?
К опухолевой трансформации приводит особый вид мутаций в генах NTRK: хромосомные перестройки, сопровождающиеся слиянием гена NTRK c геном-партнером. В результате образуется химерный белок, способный к спонтанной димеризации или мультимеризации. Химерный белок активируется внутри клетки без действия факторов роста. (Aepala 2022)
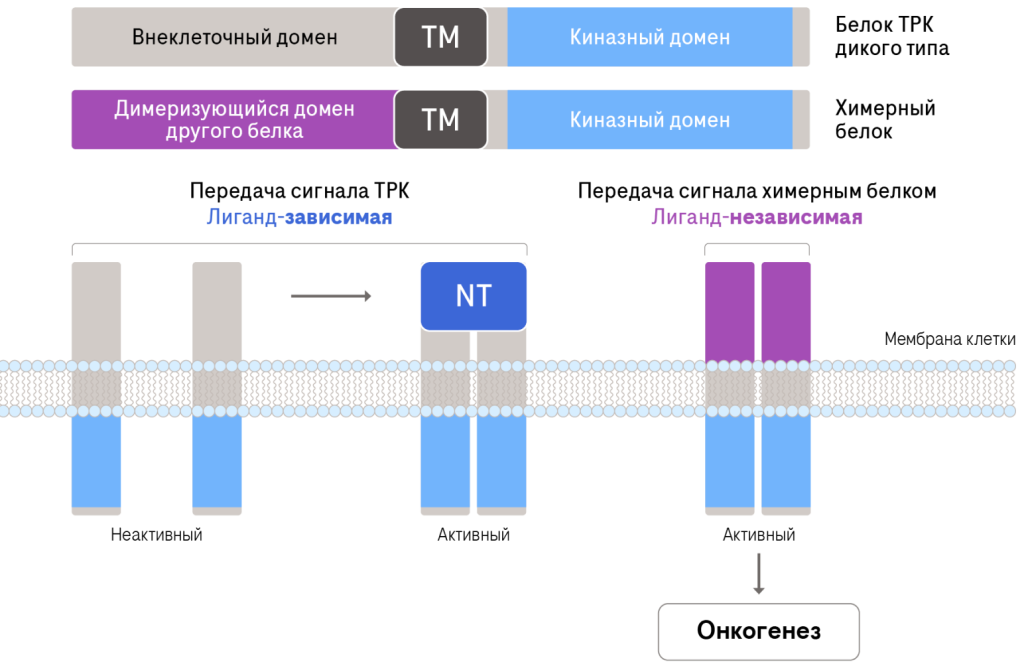
Рис. 2. Отличия химерного онкогенного белка TRK от белка TRK дикого типа. TM: трансмембранный домен, NT – нейротрофин. Иллюстрация по Farago AF (2017) J Thorac Oncol.
Таким образом, клетки, имеющие такие химерные гены NTRK, получают селективное преимущество в росте — они продолжают рост, пролиферацию и деление даже без действия факторов роста. Данное событие приводит к малигнизации и развитию NTRK-положительных опухолей. (Cocco 2018)
Для лечения опухолей с перестройками NTRK разработаны низкомолекулярные ингибиторы, блокирующие активность белков TRK. Ингибиторы TRK демонстрируют глубокие и длительные ответы при различных типах опухолей у взрослых и детей. (Desai 2022, Demetri 2022, Hong 2020)
Транслокации и точечные мутации NTRK
Показанием для назначения терапии TRK-ингибитором являются только транслокации NTRK, сопровождающиеся экспрессией химерного гена.* Эффективность и безопасность применения TRK-ингибиторов у детей изучена в ряде клинических исследований (Desai 2022) (Hong 2020), также продолжается работа по накоплению и систематизации данных о диагностике перестроек NTRK и применении TRK ингибиторов у детей в России. (Сулейманова 2019, Сергеева 2020, Корнеев 2021, Папуша 2021)
Хотя активирующие точечные мутации, амплификации и гиперэкспрессии генов NTRK могут приводить к гиперактивация нисходящих сигнальных путей и встречаются значительно чаще (Okamura 2018), данные мутации связаны с отсутствием ответа на TRK-ингибиторы (Drilon 2017, Rogers 2022)
Частота встречаемости перестроек NTRK
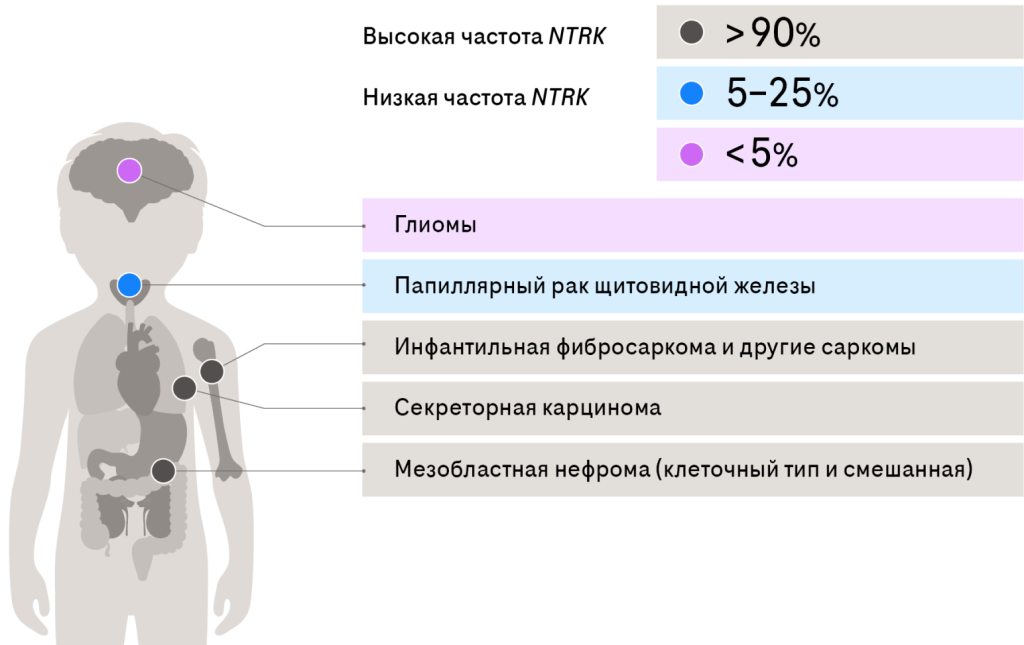
Рис. 3. Частота встречаемости перестроек NTRK при опухолях у детей. Иллюстрация по Cocco, et al. 2018; с дополнениями
Транслокации NTRK встречаются при различных типах опухолей у детей:
- C высокой частотой (>90%) при некоторых редких опухолях, таких как инфантильная фибросаркома (ИФС), врожденная мезобластная нефрома и секреторные карциномы слюнной и молочной желез. (Сулейманова 2019, Сагоян 2019, Сидоров 2020, Сагоян 2020)
- С меньшей частотой (5-25%) при инфантильных полушарных глиомах высокой степени злокачественности (Okamura 2018, Папуша 2021), папиллярном раке щитовидной железы у детей (Zhao 2021).
- Редко (<5%) встречаются при ряде сарком мягких тканей (кроме ИФС): описаны при воспалительной миофибробластической опухоли (Сулейманова 2020), злокачественной опухоли из оболочек периферических нервов (Suurmeijer 2019), а NTRK-позитивные веретеноклеточные саркомы выделены в отдельную категорию в классификации сарком ВОЗ 2020 г. (Kallen 2020) Также перестройки NTRK описаны при глиомах низкой степени злокачественности, таких как диффузная астроцитома, анапластическая пилоцитарная астроцитома, ганглиоглиома, а также при смешанной глионейральной опухоли (Zhao 2021). Перестройки NTRK могут встречаться и при других редких опухолях, например при эпителиоидной меланоцитарной опухоли (Zhao 2021).
- Исключительно редки находки перестроек NTRK при остеосаркоме, хондросаркоме, не-глиальных опухолях ЦНС, нейроэндокринных опухолях, рабдомиосаркоме (Westphalen 2021)
В то же время при эмбриональных солидных опухолях, таких как нейробластома, медуллобластома, опухоль Вильмса, атипичная тератоидно-рабдоидная опухоль, гепатобластома, не было описано транслокаций NTRK даже при анализе очень крупных когорт. (Zhao 2021, Westphalen 2021)
Каким пациентам нужно выполнять тестирование NTRK?
Исследование перестроек в генах NTRK целесообразно проводить в составе комплексной панели генов (NGS/КГП) при первично-рефрактерных, прогрессирующих или рецидивирующих солидных опухолях и редких опухолях.
Исследование перестроек в гене NTRK с помощью отдельного теста может быть оправдано при саркомах мягких тканей, при определенных опухолях ЦНС или редких опухолях, для которых транслокация в гене NTRK является частым событием. Однако стоит иметь в виду, что даже в таких “классических” опухолях как инфантильная фибросаркома, могут встречаться необычные варианты перестроек, и тестирование только одного частого варианта ETV6-NTRK3 может быть недостаточно.
Заключение
Выявление транслокаций NTRK является сложной задачей, но может предоставить пациентам дополнительные опции терапии. Обсуждение плана диагностики и лечения в рамках междисциплинарной команды может позволить рассмотреть больше возможностей диагностики и терапии для достижения лучших результатов для конкретного пациента.
Диагностика NTRK
Схемы и алгоритмы диагностики мутаций генов при солидных опухоляхКГП — комплексное геномное профилирование.
* Инструкция по применению лекарственного препарата энтректиниб
Список литературы:
- Папуша, Л.И. “Таргетная терапия инфантильных глиом полушарной локализации.” Вопросы гематологии/онкологии и иммунопатологии в педиатрии., vol. 20, no. 3, 2021, pp. 68-73.
- Сулейманова, А.М. “Новые подходы в терапии солидных опухолей у детей и подростков с использованием таргетного препарата энтректиниб.” Российский журнал детской гематологии и онкологии, vol. 6, no. 4, 2019, pp. 62-68.
- Сидоров, И.В. “Секреторная карцинома слюнных желез (аналог секреторной карциномы молочной железы) у детей.” Архив патологии, vol. 82, no. 2, 2020, pp. 43-51.
- Сагоян, Г.Б. “Врожденная мезобластная нефрома. Собственный опыт НИИ детской онкологии и гематологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России.” Российский журнал детской гематологии и онкологии (РЖДГиО), vol. 6, no. 4, 2019, pp. 25-32.
- Сагоян, Г.Б. “Врожденная инфантильная фибросаркома мягких тканей грудной стенки слева (описание клинического случая и обзор литературы).” Российский журнал детской гематологии и онкологии (РЖДГиО), vol. 7, no. 1, 2020, pp. 75-81.
- Сулейманова, А.М. “Воспалительные миофибробластические опухоли у детей: обзор литературы.” Российский журнал детской гематологии и онкологии (РЖДГиО), vol. 7, no. 2, 2020, pp. 64-77.
- Корнеев, Д.Ю. “Опыт применения препарата энтректиниб для лечения NTRK- позитивных опухолей центральной нервной системы у детей.” Российский журнал детской гематологии и онкологии, vol. II Объединенный конгресс НОДГО и РОДО, 2021, pp. 72-73.
- Сергеева, Т.В. “Первый опыт применения TRK-ингибитора энтректиниба у пациента с инфантильной фибросаркомой параменингеальной локализации.” Российский журнал оссийский журнал ДЕТСКОЙ ГЕМАТОЛОГИИ ЕТСКОЙ ГЕМАТОЛОГИИ и ОНКОЛОГИИ, vol. I Объединенный конгресс НОДГО и РОДО, 2020, p. 48.
- Aepala, M. “Nefarious NTRK oncogenic fusions in pediatric sarcomas: Too many to Trk.” Cytokine and Growth Factor Reviews, 2022.
- Cocco, E. “NTRK fusion-positive cancers and TRK inhibitor therapy.” Nature Reviews Clinical Oncology, vol. 15, 2018, pp. 731-47.
- Demetri, G. “Updated Integrated Analysis of the Efficacy and Safety of Entrectinib in Patients With NTRK Fusion-Positive Solid Tumors.” Clin Cancer Res, vol. 28, no. 7, 2022, pp. 1302-1312.
- Desai, A. “Entrectinib in children and young adults with solid or primary CNS tumors harboring NTRK, ROS1 or ALK aberrations (STARTRK-NG).” Neuro Oncol ., vol. 24, no. 10, 2022, pp. 1776-1789.
- Drilon, A. “Safety and antitumor activity of the multitargeted pan-TRK, ROS1, and ALK inhibitor entrectinib: Combined results from two phase I trials (ALKA-372-001 and STARTRK-1).” Cancer Discov, vol. 7, 2017, pp. 400-409.
- Hong, D. “Larotrectinib in patients with TRK fusion-positive solid tumours: a pooled analysis of three phase 1/2 clinical trials.” Lancet Oncol, vol. 21, no. 4, 2020, pp. 531-540.
- Kallen, M. “The 2020 WHO Classification. What’s new in soft tissue tumor pathology&.” Am J Surg Path, 2020.
- Okamura, R. “Analysis of NTRK Alterations in Pan-Cancer Adult and Pediatric Malignancies: Implications for NTRK-Targeted Therapeutics.” JCO Precis Oncol., 2018, pp. 1-20.
- Preobrazhenskaya, EV. “Gene rearrangements in consecutive series of pediatric inflammatory myofibroblastic tumors.” Pediatr Blood Cancer, vol. 67, 2020.
- Rogers, C. “NTRK point mutations and their functional consequences.” Cancer Genetics, vol. 262-263, 2022, pp. 5-15.
- Suurmeijer, A. “The histologic spectrum of soft tissue spindle cell tumors with NTRK3 gene rearrangements.” Genes Chromosomes Cancer, vol. 58, no. 11, 2019, pp. 739-746.
- Westphalen, C. “Genomic context of NTRK1/2/3 fusion-positive tumours from a large real-world population.” npj Precision Oncology, vol. 5, no. 69, 2021, pp. 1-9.
- Zhao, X. “NTRK Fusions Identified in Pediatric Tumors: The Frequency, Fusion Partners, and Clinical Outcome.” JCO Precision Oncology, vol. 5, 2021, pp. 204-214.
Сулейманова Амина Магомедовна
Дата: 10 августа 2023 г.

