Вы являетесь медицинским работником? Для полного доступа к медицинской информации войдите или зарегистрируйтесь.
Алгоритм действий врача при подозрении на рак печени
Методы визуализации и неинвазивные серологические исследования маркеров заболевания являются рекомендованными для скрининга исследованиями. Контрастная сонография (CEUS) в настоящее время не рекомендуется к использованию при проведении скрининга ГЦК. Основой скрининга является УЗИ печени каждые 4-6 месяцев у пациентов с циррозом печени или хроническим гепатитом В, способствующее выявлению очаговых узловых образований3–4.
Разработан алгоритм действий врача при обнаружении образований с пороговым значением 1 см. Использование порога в 1 см объясняется тем, что образования <1 см редко являются злокачественными. В то же время образования >1 см имеют высокую вероятность оказаться ГЦК. По сравнению с субсантиметровыми очагами образования диаметром >1 см с большей долей вероятности могут быть обнаружены при использовании методов визуализации.
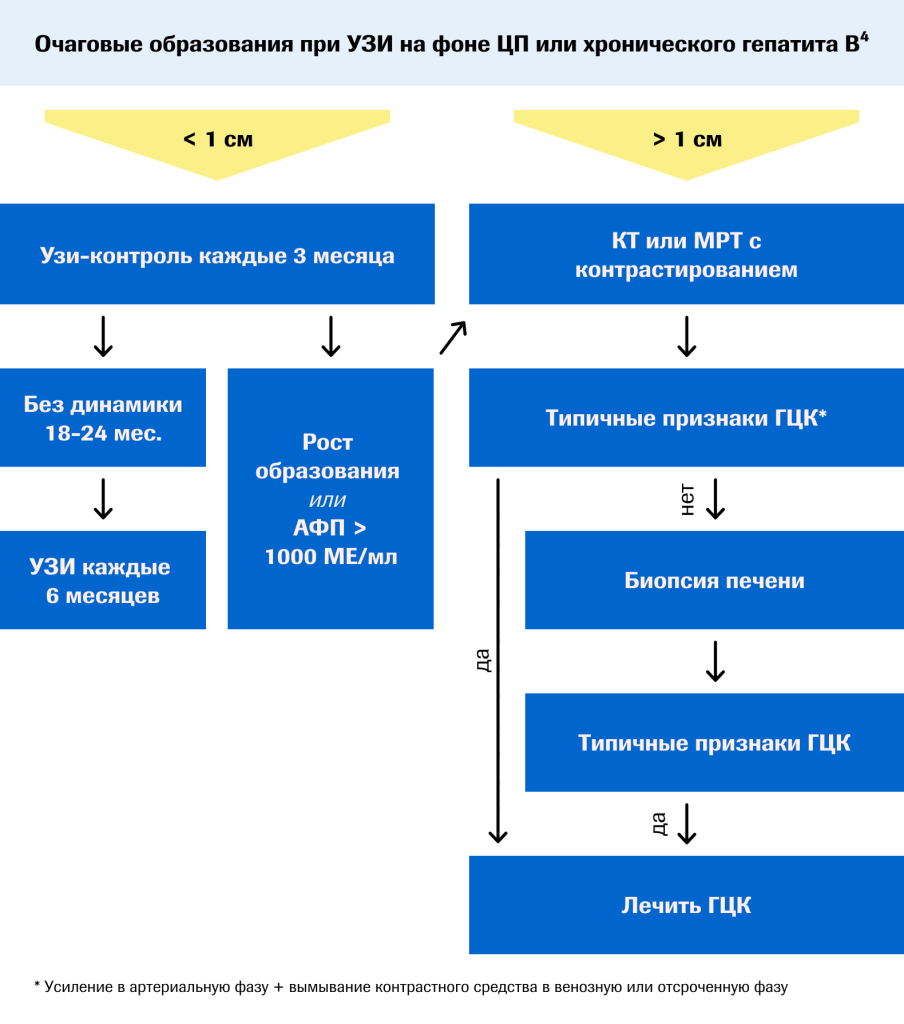
При обнаружении образования размером более 1 см (положительный результат; при этом образование не является однозначно доброкачественным) рекомендуется незамедлительное проведение уточняющих исследований, таких как КТ и/или МРТ с контрастированием. Мультиспиральная КТ печени проводится при наличии любых очаговых образований. Используется трех(четырех)фазный метод контрастирования и последующая оценка накопления контрастного средства тканью очагового образования. Характерные находки при первичном раке печени могут включать гиперваскуляризацию (контрастное усиление) в артериальную фазу исследования и вымывание контрастного средства в венозную фазу3–4.
При обнаружении данных диагностических признаков и и/или уровне маркера опухоли альфа-фетопротеина (АФП) выше 400 нг/мл пациенту показано лечение ГЦК. Также тест на АФП считают положительным, если его значение >20 нг/мл и отрицательным, если ниже. Как считается, этот порог обеспечивает чувствительность около 60% и специфичность около 90% при условии 5% распространенности ГЦК в изучаемой выборке, что должно давать 25% положительную прогностическую ценность для диагностики5. Кроме того, в последнее время для проведения скрининга были предложены также другие биомаркеры, такие как глипикан-3 (GPC-3), фракция AFP-L3 и протромбин, вызванный отсутствием витамина К II (PIV II или DCP), однако все они в настоящее время не рекомендуются для практического использования и требуют дальнейшего изучения2. Мелкие высокодифференцированные опухоли не приводят к увеличению уровня АФП на раннем этапе своего развития, поэтому нормальный АФП не свидетельствует об отсутствии ГЦК. С другой стороны, так как АФП является неспецифическим белком, его уровень может значительно повышаться у пациентов с активным HCV- или HBV- гепатитом, или в ответ на другое хроническое воспаление печени. Это часто является причиной ложноположительных результатов скрининга.
При недостаточной диагностической точности КТ проводится МРТ, значительно превосходящая КТ по своей чувствительности. Также МРТ или многофазная МСКТ могут применяться для проведения скрининга у пациентов с ожирением, повышенным газообразованием, деформацией грудной стенки или перенесенными ранее вмешательствами, ухудшающими УЗИ-визуализацию.
В случае отсутствия типичных признаков ГЦК в очаговом образовании печени рекомендуется биопсия опухолей размером <2 см, далее пациент направляется на иммуногистохимическое и генетическое типирование. Если при этом будут выявлены диагностические признаки ГЦК, пациенту назначается терапия ГЦК.
При обнаружении образования размером менее 1 см (неуточненный результат; при этом образование не является однозначно доброкачественным) проводится УЗИ- контроль каждые 3 месяца. В случае отсутствия динамики в течение 18-24 месяцев рекомендуется проведение УЗИ через каждые полгода. При росте образования или уровне АФП, увеличивающего вероятность выявления ГЦК на ранних стадиях на 6-8 %, >1000 МЕ/мл пациент направляется на КТ и/или МРТ с контрастированием с последующими этапами обследований, описанными выше4–5.
В случае отрицательного результата (когда в печени отсутствуют очаговые патологические образования, или если эти образования являются однозначно доброкачественными) пациент отправляется на дальнейшее наблюдение с повторным осмотром через полгода. Интервал наблюдения зависит от медианы времени удвоения опухоли, которая для ГЦК составляет 80-117 дней1.
Таким образом, у пациентов группы риска скрининг должен проводиться 1 раз в 6 месяцев с использованием УЗИ + АФП, что рекомендуется всеми ведущими ассоциациями3,5–6.
ГЦК – гепатоцеллюлярная карцинома, ЦП – цирроз печени, HBV – вирус гепатита B, HCV – вирус гепатита С, EASL – European Association for the Study of the Liver, APASL – Asian-Pacific Association for the Study of the Liver, AASLD – American Association for the Study of Liver Disease, УЗИ – ультразвуковое исследование, КТ – компьютерная томография, МСКТ – мультиспиральная компьютерная томография. МРТ – магнитно-резонансная томография, CEUS – Contrast-Enhanced Ultrasound, АФП – альфа-фетопротеин, PIVKA-II — protein induced by vitamin K absence, DCP – des-gamma carboxyprothrombin, GPC-3 – глипикан-3
Источники:
- Ивашкин В.Т.. Маев И.В., Каприн АД.. Агапов М.Ю.. Андреев Д.Н.. Водолеев А.С.. Жаркова М.Ю.. Королев М.П.. Кучерявый Ю.А. Лапина Т.Л., Маевская М.В., Охлобыстин А.В.. Павлов Ч.С.. Параскевова АВ.. Пирогов С.С., Полуэктова Е.А. Румянцева Д.Е.. Трухманов АС., Царьков П.В.. Шептулин АА, Шифрин О.С. Раннее выявление онкологических заболеваний органов пищеварения (методическое руководство Российской гастроэнтерологической ассоциации и Ассоциации онкологов России для врачей первичного звена здравоохранения). Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2019. — 29 (5):67-6S. https://doi.org/10.22416/13S2-4376-2019-29-5-53-74
- Балахнин П.В., Шмелев АС.. Шачинов Е.Г.. Малькевич В.И. Этиология, скрининг и ранняя диагностика гепатоцеллюлярного рака: успехи и новые вызовы, связанные с эпидемией ожирения. — Практическая онкология. — 2019. — Т. 20. № з. — С. 196-197.
- European Association for the Study of the Liver. EASL Clinical Practice Guidelines: Management of hepatocellular carcinoma. J. Hepatol. 2018;69:182–236.
- Тихонов И.Н., Павлов Ч.С., Маевская М.В., Ивашкин В.Т. Современные подходы к скринингу и ранней диагностике гепатоцеллюлярной карциномы. Современная онкология. 2014;3:65–74. [Tikhonov I.N., Pavlov Ch.S., Mayevskaya M.V., Ivashkin V.T. Modern approaches to screening and early diagnosis of hepatocellular carcinoma. Modern Oncology. 2014;3:65–74 (In Rus.)].
- Marrero J.A., Kulik L.M., Sirlin C.B., Zhu A.X., Finn R.S., Abecassis M.M., Roberts L.R., Heimbach J.K. Diagnosis, Staging, and Management of Hepatocellular Carcinoma: 2018 Practice Guidance by the American Association for the Study of Liver Diseases // Hepatology. – 2018. – Vol. 68, № 2. – P. 723–750.
- Omata M., Cheng A.L., Kokudo N., Kudo M., Lee J.M., Jia J., Tateishi R., Han K.H., Chawla Y.K., Shiina S., Jafri W., Payawal D.A., Ohki T., Ogasawara S., Chen P.J., Lesmana C.R.A., Lesmana L.A., Gani R.A., Obi S., Dokmeci A.K., Sarin S.K. Asia-Pacific clinical practice guidelines on the management of hepatocellular carcinoma: a 2017 update // Hepatol Int. – 2017. – Vol. 11, № 4. – P. 317–370.

