Вы являетесь медицинским работником? Для полного доступа к медицинской информации войдите или зарегистрируйтесь.
Системная терапия дифференцированного рака щитовидной железы: что нового в рекомендациях ESMO 2022?
Румянцев Павел Олегович
д.м.н., профессор, главный онколог-радиолог, заместитель главного врача Клиники высоких технологий «Белоостров» ММЦ-ВТ, Группа компаний «Мой медицинский центр», г. Санкт-Петербург
В апреле 2022 года опубликованы обновленные рекомендации ESMO по использованию системной терапии при местнораспространенном и метастатическом раке щитовидной железы, не подлежащего хирургическому или другому локальному лечению1. Рекомендации включают лечение дифференцированного рака щитовидной железы (ДРЩЖ), рефрактерного к терапии радиоактивным йодом, а также лечение анапластического и медуллярного рака.
В 2013 году мультикиназный ингибитор (МКИ) сорафениб получил одобрение FDA для лечения местнораспространенного или метастатического ДРЩЖ, рефрактерного к терапии радиоактивным йодом2. Затем в 2015 последовало одобрение другого МКИ — ленватиниба3. За прошедшие годы МКИ ленватиниб и сорафениб стали стандартной терапией для данной группы пациентов4.
Обновленные рекомендации ESMO 2022 приводят накопленные данные о применении МКИ и описывают новые фармакологические стратегии с использованием селективных ингибиторов тирозинкиназ для лечения пациентов с ДРЩЖ1.
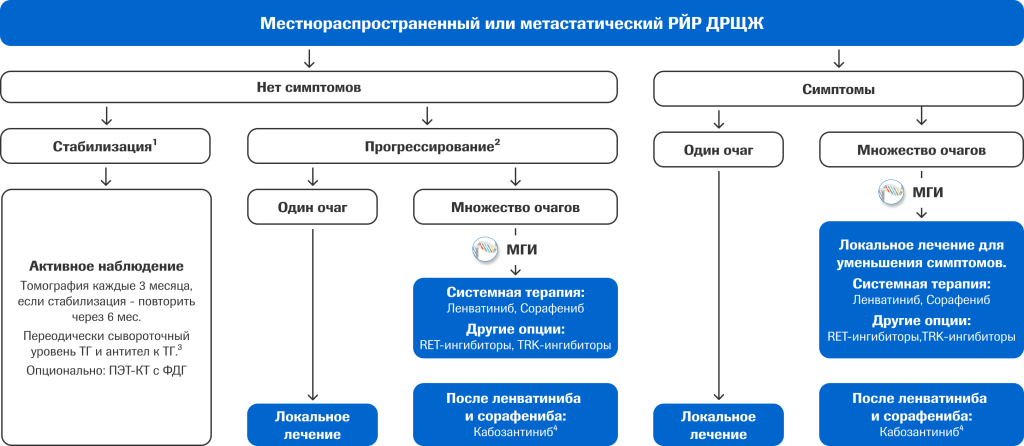
Рис. 1. Рекомендации по ведению пациентов с радиойод-рефрактерным, распространенным или метастатическим ДРЩЖ1.
RET — рецептор RET, продукт гена RET; TRK — семейство рецепторов TRK, продукты генов NTRK1-3. ДРЩЖ — дифференцированный рак щитовидной железы, МГИ — молекулярно-генетические исследования, ПЭТ КТ с ФДГ — позитронно-эмиссионная томография с фтордезоксиглюкозой, РЙР — рефрактерный к терапии радиоактивным йодом, ТГ — тиреоглобулин.
- Большая опухолевая нагрузка может потребовать локальной или системной терапии.
- По критериям RECIST v1.1
- Динамика уровней ТГ или антител к ТГ в сыворотке крови, а также их поглощение при ПЭТ КТ с ФДГ могут быть предикторами прогрессирования заболевания.
- Данное показание кабозантиниба не зарегистрировано в РФ
Накопленный опыт применения МКИ соответствует данным РКИ
Эффективность и безопасность МКИ изучалась в двух рандомизированных клинических исследованиях (РКИ): SELECT (исследование ленватиниба при дифференцированном раке щитовидной железы, рефрактерном к 131I) и DECISION (исследование сорафениба у пациентов с местнораспространенным или метастатическим раком щитовидной железы, рефрактерным к радиоактивному йоду)5,6. По данных этих РКИ ленватиниб и сорафениб увеличивают медиану выживаемости без прогрессирования (ВБП) по сравнению с плацебо: 18,3 месяца (ленватиниб) против 3,6 месяца (плацебо) и 10,8 месяца (сорафениб) против 5,8 месяца (плацебо)5,6. Кроссовер был разрешен в обоих исследованиях и составил ≥ 75%, что повлияло на результаты общей выживаемости (ОВ)7. После коррекции данных ОВ с учетом кроссовера, авторы исследований сообщили о статистически значимом улучшении ОВ у пациентов, получавших ленватиниб, по сравнению с плацебо, но не было получено различий в ОВ между группами сорафениба и плацебо7. И ленватиниб, и сорафениб увеличивают частоту нежелательных явлений (НЯ), требуется снижение дозы для > 60% пациентов7. По сравнению с плацебо или наилучшей поддерживающней терапией лечение ленватинибом или сорафенибом приводит к увеличению ВБП, частоты объективного ответа опухоли и, возможно, ОВ, но для лечения НЯ часто требуется модификация дозы7.
Данные реальной клинической практики подтверждают эффективность МКИ и соответствие их профиля безопасности данным РКИ. Результаты девяти проспективных обсервационных исследований и 13 систематических обзоров ленватиниба или сорафениба в целом сопоставимы с результатами РКИ7. Однако между исследованиями выявляются существенные различия в величине показателей эффективности и частоте некоторых нежелательных явлений. Авторы связывают различия с неоднородностью исследований по критериям включения, размеру выборки, дозам препаратов, продолжительности наблюдения, оценке прогрессирования заболевания и анализе результатов1.
На основании имеющихся в настоящее время данных не может быть определена оптимальная последовательность назначения данных МКИ1. Прямое сравнение ленватиниба и сорафениба никогда не проводилось, что не позволяет установить иерархию между ними2. Когда обе терапевтические стратегии возможны, решение должно приниматься на основании ожидаемого ответа на лечение, профиля безопасности препарата и предпочтений пациента1.
Снижение дозы может приводить к снижению эффективности
Учитывая токсичность, связанную с МКИ, в реальной клинической практике иногда предпочитают начинать лечение с более низкой дозы, чем утвержденная1. В недавнем РКИ сравнивали профиль эффективности и безопасности ленватиниба в утвержденной начальной дозе (т. е. 24 мг в сутки) и в более низкой начальной дозе (т. е. 18 мг в сутки) в когорте пациентов с метастатическим/распространенным ДРЩЖ8. Более высокая доза оказалась более эффективной: частота объективного ответа (ЧОО) составила 57,3% по сравнению с 40,3% в группе с более низкой дозой [отношение шансов 0,50 (95% ДИ 0,26-0,96)]8. Профиль безопасности был сопоставим8. Хотя эти данные нельзя обобщать на весь класс МКИ, представляется разумным утверждать, что чем выше доза, тем выше эффективность этих препаратов1. Хотя это предположение поддерживает использование утвержденной начальной дозы МКИ для максимизации их эффективности, выбор должен быть индивидуализирован в зависимости от общего состояния пациента и сопутствующих заболеваний1.
Добавлены молекулярно-генетические исследования перед назначением системной терапии
Если планируется системная терапия местнораспространенного или метастатического ДРЩЖ, для терапии следует рассмотреть выполнение молекулярно-генетических исследований драйверных мутаций для назначения персонализированной таргетной системной терапии1. Анализ методом секвенирования следующего поколения на основе РНК (РНК NGS) является предпочтительным, если он доступен1.
Добавлены RET-ингибиторы
Два селективных ингибитора RET одобрены в США и один из них в настоящее время одобрен в ЕС для лечения распространенного/метастатического рака щитовидной железы с перестройками гена RET. Данный класс препаратов добавлен в схему системной терапии ДРЩЖ в обновленных рекомендациях ESMO.1
Добавлены TRK-ингибиторы
Ингибиторы TRK одобрены в США, ЕС и ряде других стран для лечения солидных опухолей с перестройками генов NTRK, включая рак щитовидной железы. Данный класс препаратов добавлен в схему системной терапии ДРЩЖ в обновленных рекомендациях ESMO.1
Список литературы:
- S. Filetti et al. ESMO Clinical Practice Guideline update on the use of systemic therapy in advanced thyroid cancer. Annals of Oncology. 2022
- Nexavar FDA Approval History: Approval FDA Approves Nexavar to Treat Metastatic Differentiated Thyroid Cancer 2013. https://www.drugs.com/history/nexavar.html Доступ от 14 июля 2022 г.
- Lenvima FDA Approval History: Approval FDA Approves Lenvima (lenvatinib) for Differentiated Thyroid Cancer 2015. https://www.drugs.com/history/lenvima.html Доступ от 14 июля 2022 г.
- Рубрикатор клинических рекомендаций. Дифференцированный рак щитовидной железы 2020. https://cr.minzdrav.gov.ru/recomend/329_1 Доступ от 14 июля 2022 г.
- Brose, M. S. “Sorafenib in radioactive iodine-refractory, locally advanced or metastatic differentiated thyroid cancer: a randomised, double-blind, phase 3 trial.” Lancet, vol. 384, no. 9940, 2014, pp. 319-28.
- Schlumberger, M. “A phase 3, multicenter, double-blind, placebo-controlled trial of lenvatinib (E7080) in patients with 131I-refractory differentiated thyroid cancer (SELECT).” NEJM, vol. 372, 2015, pp. 621-30.
- Fleeman N, Houten R, Bagust A et al. Lenvatinib and sorafenib for differentiated thyroid cancer after radioactive iodine: a systematic review and economic evaluation. Health Technol Assess 2020; 24 (2): 1-180.
- Brose MS, Panaseykin Y, Konda B et al. A Randomized Study of Lenvatinib 18 mg vs 24 mg in Patients With Radioiodine-Refractory Differentiated Thyroid Cancer. J Clin Endocrinol Metab 2022; 107 (3): 776-787.

